Photpho ( P ) hóa trị mấy? ứng dụng và tính chất của P – Svnckh
Trong bài viết này viethanbinhduong.edu.vn sẽ chia sẻ chuyên sâu kiến thức của Photpho hóa trị mấy để chia sẻ cho bạn đọc
Photpho (P) là một nguyên tố quan trọng của sự sống. Nó kết hợp với oxy để tạo ra phosphate, hợp chất đóng vai trò tạo ra liên kết trong ADN, làm xương chắc khỏe và thực hiện các phản ứng hóa học bên trong tế bào con người. Photpho nguyên chất có nhiều dạng và màu sắc như trắng, đỏ, tím, đen, hồng, tùy thuộc vào sự sắp xếp của các nguyên tử. Trong bài này chúng ta cùng tìm hiểu xem Photpho ( P ) hóa trị mấy? ứng dụng và tính chất của P như thế nào.
Thông tin cơ bản về Photpho :
Hóa Trị của P : có thể là 5. Ngoài ra, trong một số hợp chất, photpho còn có hóa trị 3.
Số nguyên tử :Photpho ở ô thứ 15, nhóm VA, chu kì 3 trong bảng tuần hoàn.
Ký hiệu: P
Trọng lượng nguyên tử : 30,973762
Khám phá: Thương hiệu Hennig, 1669 (Đức)
Cấu hình electron : [Ne] 1s22s22p63s23p3
Từ Nguồn gốc: Tiếng Hy Lạp: photphoros: mang ánh sáng, cũng là tên cổ xưa được đặt cho hành tinh Venus trước khi mặt trời mọc.
Tính chất của photpho :
Tính chất vật lý :
Photpho có thể tồn tại ở một số dạng thù hình khác nhau, nhưng quan trọng hơn cả là photpho trắng và photpho đỏ.
1. Photpho trắng
– Là chất rắn trong suốt, màu trắng hoặc hơi vàng, trông giống như sáp, có cấu trúc mạng tinh thể phân tử. Trong tinh thể, những phân tử P4 nằm ở nút mạng và liên kết với nhau bằng lực tương tác yếu như hình vẽ:
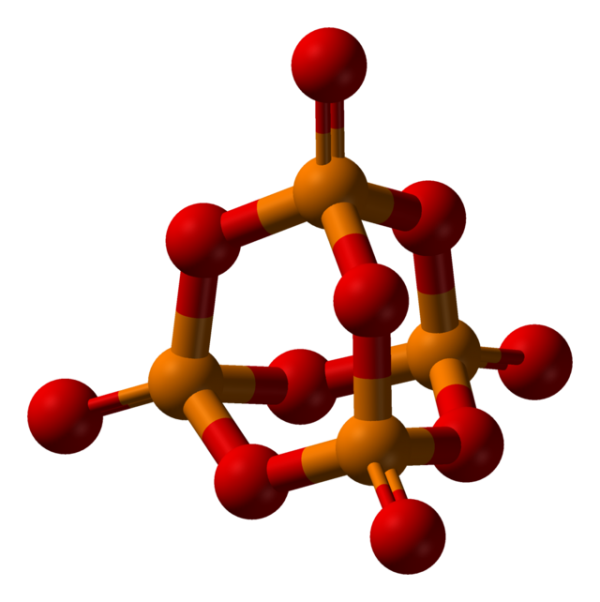
– Mềm, dễ nóng chảy (tnc = 44,1oC).
– Không tan trong nước, tan trong một số dung môi hữu cơ như C6H6, CS2, … ;
- Natri có hóa trị mấy ( Na ) ? nguyên tử khối của Natri
- Flo hóa trị mấy ( F ), Định nghĩa và Tính chất của Flo như thế nào?
- Oxi có mấy hóa trị ( O ), Đặc điểm và vai trò của oxi
– Rất độc và gây bỏng nặng khi rơi vào da.
– Bốc cháy trong không khí ở nhiệt độ trên 40oC, nên được bảo quản bằng cách ngâm trong nước.
-Phát quang màu lục nhạt trong bóng tối ở nhiệt độ thường.
– Khi đun nóng đến nhiệt độ 250oC và không có không khí, photpho trắng chuyển dần thành photpho đỏ là dạng bền hơn.
2. Photpho đỏ
– Là chất bột màu đỏ, dễ hút ẩm và chảy rữa, bền trong không khí ở nhiệt độ thường và không phát quang trong bóng tối.
– Không tan trong các dung môi thông thường.
– Bốc cháy ở nhiệt độ trên 250oC.
– Khi đun nóng không có không khí, photpho đỏ chuyển thành hơi, khi làm lạnh thì hơi đó ngưng tụ lại thành photpho trắng.
– Có cấu trúc polime nên khó nóng chảy và khó bay hơi hơn photpho trắng.

Tính chất hóa học :
Photpho là phi kim tương đối hoạt động. Photpho trắng hoạt động hóa học mạnh hơn photpho đỏ. Trong các hợp chất, photpho có số oxi hóa -3, +3 và +5. Do đó, khi tham gia phản ứng hóa học photpho thể hiện tính oxi hóa hoặc tính khử.
1. Tính oxi hóa
Tác dụng với một số kimloại hoạt động tạo ra photphua kim loại.
2. Tính khử
Tác dụng với các phi kim hoạt động như oxi, halogen, lưu huỳnh,… và các hợp chất có tính oxi hóa mạnh khác.
Photpho cháy được trong không khí khi đốt nóng:

Công dụng của P :
Phốt pho đỏ, tương đối ổn định, được sử dụng để làm diêm an toàn , đạn đánh dấu, thiết bị gây cháy, thuốc trừ sâu, thiết bị bắn pháo hoa và nhiều sản phẩm khác. Nhu cầu phốt phát cao để sử dụng làm phân bón. Phốt phát cũng được sử dụng để chế tạo một số loại kính (ví dụ: dùng cho đèn natri). Trisodium phosphate được sử dụng như một chất làm sạch, làm mềm nước và chất ức chế cáu cặn / ăn mòn. Tro xương (canxi photphat) được dùng để làm đồ sành sứ và làm monocalcium photphat làm bột nở. Phốt pho được sử dụng để làm thép và đồng phốt pho và được thêm vào các hợp kim khác. Có rất nhiều công dụng đối với các hợp chất photpho hữu cơ.
Sản xuất
Photpho đỏ được sản xuất bằng cách nung hỗn hợp quặng photphorit (hoặc apatit), cát và than cốc ở 1200 oC trong lò điện. Hơi photpho thoát ra được ngưng tụ khi làm lạnh, sẽ thu được photpho trắng ở dạng rắn.
Trạng thái tự nhiên
– Trong tự nhiên có hai khoáng vật chính của photpho là photphorit Ca3(PO4)2 và apatit 3Ca3(PO4)2.CaF2. Nước ta có mỏ apatit ở Lào Cai, một số mỏ photphorit ở Thái Nguyên, Thanh Hóa, …
– Ngoài ra, photpho có trong protein thực vật; trong xương, răng, bắp thịt, tế bào não, … của người và động vật.
Xem thêm hóa trị của các nguyên tố tại bảng hóa trị sau :
Bảng Hóa Trị Lớp 8, Cách Học Thuộc Bằng Bài Ca Hóa Trị Hóa Học.
Silic ( Si ) hóa trị mấy? Tính chất hóa học và ứng dụng của Silic
Nhôm hóa trị mấy? kí hiệu và nguyên tử khối của Al
Magie có hóa trị mấy ( Mg )? Tính chất hóa học và nguyên tử khối của Mg

