Flo hóa trị mấy ( F ), Định nghĩa và Tính chất của Flo như thế nào?
Trong bài viết này viethanbinhduong.edu.vn sẽ chia sẻ chuyên sâu kiến thức của Flo hóa trị mấy để chia sẻ cho bạn đọc
Bảng hóa trị của các nguуên tố hóa học là tài liệu kiến thức nhập môn hóa học 8.Trong bảng tuần hoàn hóa học flo đứng Flo là nguyên tố phi kim và cũng là nguyên tố hóa học hoạt động mạnh nhất. . Vì thế nó mang lại những mặt tích cực lẫn tiêu cực cho con người, Vậy Flo có hóa trị mấy, Định nghĩa và tính chất của flo như thế nào, ở dưới bài viết này chúng ta cùng nhau đi tìm hiểu rõ về nguyên tố này nhé.
Khí Flo là gì?
Flo (tên tiếng anh: Flour) là một chất khí thuộc halogen,
Vị trí và cấu tạo của nguyên tử:
– Ký hiệu hóa học: F.
– Nguyên tử khối: 18,998 g/mol (thường lấy là 19 g/mol).
– Số đơn vị điện tích hạt nhân: Z = 9.
– Độ âm điện: 3,98 (nguyên tố có độ âm điện lớn nhất).
-Hóa trị của Flo : I
– Số oxi hóa: -1
– Cấu hình: 1s22s22p5.
=> Vị trí: ô số 9; chu kỳ 2; nhóm VIIA.
– Bán kính nguyên tử (nm): 0,64.
– Có 7e lớp ngoài cùng → cấu hình e lớp ngoài cùng là ns2np5 -> .
– Ở trạng thái cơ bản, Flo chỉ thiếu 1 e đạt cấu hình e bền vững của khí hiếm => dễ dàng nhận 1e để tạo thành ion âm F‑ hoặc tạo 1 liên kết CHT với 1 nguyên tử F khác tạo F2.
– Đơn chất Flo tồn tại ở dạng phân tử do 2 nguyên tử F kết hợp với nhau bằng liên kết CHT tạo thành (F2).
- Hóa trị của Beri ( Be), Tính chất và hợp chất chuẩn của Be
- Hóa trị của liti ( Li ), tính chất hóa học và khối lượng nguyên tử
– Trong các hợp chất, Flo có số oxi hóa là -1 và không có số oxi hóa dương (vì Flo có độ âm điện lớn nhất và trong cấu hình e chưa xuất hiện phân lớp 3d, vì vậy dù ở trạng thái kích thích thì flo chỉ có 1 electron lớp ngoài cùng, chỉ có khả năng nhận thêm một electron để đạt đến cấu hình của khí hiếm Neon).
Flo trong tự nhiên: Trong tự nhiên, Flo không tồn tại ở dạng đơn chất mà tồn tại ở hợp chất.
Hợp chất của flo còn xuất hiện trong men răng của người và động vật, ngoài ra còn có trong lá của 1 số loài thực vật. 2 khoáng vật chứa nhiều flo là Florit (CaF2) và Criolit (Na3AlF6). Flo chiếm 0,08% khối lượng vỏ Trái Đất, đây là một tỉ lệ khá nhiều hơn một vài nguyên tố như đồng, kẽm,…
Tính chất của nguyên tố Flo :
Tính chất vật lí của Flo
Màu sắc Vàng lục nhạt Trạng thái khí Nhiệt độ nóng chảy -219,62 C Nhiệt độ sôi -118,12 C Độc tính Rất độc, mức độ chết người
Tính chất hóa học của Flo
Có 3 phản ứng tiêu biểu nhất khi nhắc đến tính chất hóa học của Flo là:
Tác dụng với kim loại và phi kim Flo tác dụng tất cả kim loại kể cả Au và Pt, đồng thời cũng phản ứng được hầu hết phi kim (trừ O2 N2 và các nguyên tố khí trơ)
Ca + F2 → CaF2
3F2 + S → SF6
3F2 + 2Au → AuF3 (Vàng florua)
F2 + Cu → CuF2 (Đồng (II) florua)

Tính chất hóa hóc Flo
Tác dụng với hidro: – Flo phản ứng hóa học mạnh với hidro hơn các halogen khác tạo ra axit flohydric. Phản ứng nổ rất mạnh, có thể ngay cả trong bóng tối, nhiệt độ thấp. Gây chêt người
H2 + F2 → 2HF
– Khí HF kết hợp với nước sẽ tạo ra dung dịch HF – đây là loại axit yếu. Dung dịch HF được ứng dụng trong kĩ thuật khắc thủy tinh. Vì khi nó tác dụng với SiO2 sẽ tạo dung dịch có khả năng ăn mòn thủy tinh.
SiO2 + 4HF → SiF4 (Silic tetrafloru) + 2H2O
- Hidro (H) hóa trị mấy? Nguyên tử khối và tính chất hóa học
Khí flo qua nước sẽ làm bốc cháy nước (do giải phóng O2).
2F2 + 2H2O → 4HF + O2
Đó cũng là nguyên nhân vì sao F2 không đẩy Cl2, Br2, I2 ra khỏi dung dịch muối hoặc axit mặc dù flo có tính oxi hóa mạnh hơn.
Phản ứng Trao đổi Tương tự kim loại mạnh đẩy kim loại yếu ra khỏi dung dịch muối, flo có khả năng thế chỗ các halogen khác ra khỏi các hợp chất ion hoặc hợp chất công hóa trị
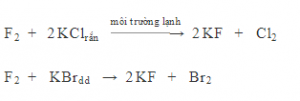
Nếu dư F2 còn có phản ứng:
Br2 + 5F2 + 6H2O → 2HBrO3 + 10HF
và có một phần flo tác dụng với H2O
Phản ứng này giải thích vì sao F2 không đẩy Cl2, Br2, I2 ra khỏi dung dịch muối hoặc axit trong khi flo có tính oxi hóa mạnh hơn.
Phản ứng với các dung dịch kiềm Khác với các halogen khác, flo không tạo muối chứa oxi. Khi phản ứng với kiềm loãng (thí dụ NaOH 2%) lạnh tạo ra Oxidiflorua và muối florua

Cách điều chế Flo
– Vì flo là nguyên tố hóa học có tính oxi hóa mạnh nhất nên không có bất cứ chất nào có khả năng oxi hóa nó được nữa. Nên cách duy nhất để sản xuất ra khí flo là điện phân nóng chảy KF và HF.
– Bình điện phân chứa hỗn hợp KF và HF sẽ có cực âm bằng thép đặc biệt hay đồng và cực dương bằng than chì. Khi phản ứng xảy ra, khí hiđro thoát ra ở cực âm và khí flo thoát ra ở cực dương.
Hi vọng qua bài này, các bạn sẽ nhận được một lượng kiến thức cơ bản về khí Flo.
Ứng dụng
Điều chế dẫn xuất flo để sản xuất chất dẻo. Dùng trong công nghiệp hạt nhân để làm giàu 235U. Dung dịch NaF loãng được dùng làm thuốc chống sâu răng. Dùng làm chất oxi hóa cho nhiên liệu lỏng dùng trong tên lửa. Dung dịch NaF loãng dùng làm thuốc chống sâu răng. Dùng trong công nghiệp sản xuất hạt nhân.
Những tác hại mà flo gây ra cho con người
Sử dụng thực phẩm chứa flo một thời gian dài gây mủn răng, hư hại răng. Tăng tỉ lệ bị ròn xương hay gãy của xương vì Flo trong thức ăn sẽ lấy canxi trong xương. Ngoài ra nó còn lấy canxi có trong máu khiến xuất hiện các bệnh như co cứng cơ, suy tim mạch.
Không chỉ mỗi khí flo gây độc, một vài hợp chất của nó như HF, khi con người hít phải cũng gây nhiều bệnh. Một số triệu chứng tiêu biểu như đau xương ức, ho ra đờm, máu, phù nề phổi. Các bộ phận trong cơ thể nếu những khí đó tiếp xúc, đi qua. Điều chế một số hợp chất của nó cũng gây bao nhiêu phiền toái: gây nổ, bỏng, cháy,…
Xem thêm tại đây :
Bảng Hóa Trị Lớp 8, Cách Học Thuộc Bằng Bài Ca Hóa Trị Hóa Học.
Oxi có mấy hóa trị ( O ), Đặc điểm và vai trò của oxi
Nitơ ( N ) hóa trị mấy? Cấu tạo phân tử của N
Hóa trị của Cacbon là mấy ( C ), Nguyên tử khối và cách điều chế chuẩn
Hóa trị của nguyên tố Bo ( B ), Tính chất và vai trò của nguyên tố B


